─AD─
ウイルスクリアランス試験の受託サービスを開始
バイオ医薬品開発のウイルス安全性評価を強力支援
ユーロフィン分析科学研究所

グローバル展開するユーロフィングループのユーロフィン分析科学研究所は、年間3,000件以上に及ぶ多様な受託試験サービスを提供している。欧米のEurofins BPT(BioPharma Product Testing)ネットワークと緊密に連携し、国際的な品質基準に準拠した高品質な試験データを通じて、製薬企業の研究開発を強力に支援している。その同社が2026年7月より、ウイルスクリアランス試験の国内受託サービスを開始する。
本稿では、新サービスの立ち上げを牽引する事業開発部の金森貴宏氏に、同社のウイルスクリアランス試験の概要や支援について話を聞いた。
■アクセス性に優れた神戸ポートアイランドに専用ラボを設置
ユーロフィン分析科学研究所は、日本国内の医薬品分析およびバイオファーマサービスの中核拠点を担い、グループで蓄積された知見を基に、高品質な分析技術でさまざまな企業をサポートしてきた実績を有する。
同社では、国内ユーザーから高いニーズに応える形で“ウイルスクリアランス試験”の国内受託サービスを2026年7月、アクセスに優れた神戸ポートアイランドの専用ラボで開始する。

「国内ラボで試験を実施することで、時差のない環境で日本語による円滑なコミュニケーションが可能になります。立ち会い実験に伴う渡航コストや時間を大幅に削減できる点も大きなメリットです」と、米国ユーロフィングループのラボでウイルスクリアランス試験に関するグローバルスタンダードの技術研修を受けた金森氏は、国内実施ならではの利便性と付加価値を強調する。
■グループでは約20年前からウイルスクリアランス試験を受託
バイオ医薬品の開発・製造において、ウイルス安全性の確保は極めて重要である。ウイルスクリアランス試験は、バイオ医薬品の製造工程において、ウイルスの不活化または除去能力を定量的に評価する試験で、治験開始時や医薬品の承認申請時に必要とされ、製品の安全性管理において重要な役割を果たす。
試験では、製造工程の各ステップにウイルスを意図的に添加し、各工程を経る中でウイルスがどの程度不活化または除去されるかを評価する。複数の工程で十分なクリアランスが確認できれば、必ずしもすべての工程を評価する必要はないとされている。
ユーロフィングループでは、約20年前からGMPに準拠したウイルスクリアランス試験を受託し、医薬品開発の各段階で幅広く支援してきた実績をもつ。ウイルスクリアランス試験では、レトロウイルスやパルボウイルスなどのモデルウイルスの感染性を保持したまま操作するため、BSL-2~BSL-3レベルの専用施設が求められる。そのような制約から、日本国内ではこうした施設・実績を持つCROが非常に少なく、実績のある海外のCROに委託するケースが多かった。
「ユーロフィングループは、世界60カ国以上でサービスを提供しています。われわれは海外拠点と密接に連携し、開発から商業生産まで、熟練した技術をもつ専門家が分析サポートを提供しています。各国のレギュレーションに対応しており、低分子からバイオ医薬品まで幅広くサポートし、E&Lやニトロソアミンなどの不純物試験なども受託しています。国内でもバイオ医薬品の開発プロジェクトが増えており、ウイルスクリアランス試験の需要が急速に高まっていることを受け、さらなるサービス拡充のためにウイルスクリアランス試験の受託体制を整備することにしました」(金森氏)。
■コスト削減、開発期間短縮でバイオ医薬品の開発力アップ
ウイルスクリアランス試験で使用されるウイルスは、製品を汚染する可能性があるウイルスと同等とみなされるものが選定され、試験目的や各国のガイドラインに基づき、ウイルス選択の妥当性を示すことが求められる。
また、実際の製造工程をスケールダウンした条件で実施され、通常2工程以上の製造工程について評価し、それぞれの工程がどの程度のウイルス不活化・除去能力を有しているか確認する。この製造工程をスケールダウンする際には、試験委託者である製薬企業の製造ノウハウが必須であるため、ウイルスクリアランス試験の際には、委託者も立ち会い、プロセスを組み立てるケースが多いという。
「ウイルスクリアランスの試験の性質上、短くても約1週間、製薬企業の担当者が立ち会うことになるため、海外渡航費などでコストがかかります。神戸というアクセスが容易なラボで試験ができれば、こうしたコストも削減できます」(金森氏)。
欧米のEurofins BPTが提供するウイルスクリアランス試験受託サービスは、①レベル1のベーシックサービスは顧客がユーロフィンのウイルスクリアランス施設にてすべての工程を実施、②レベル2のグレードアップサービスでは、クロマトグラフィー工程およびフィルトレーション工程は顧客が実施し、ウイルス不活化工程をユーロフィンが担当、③レベル3のフルカバーサービスは顧客から技術移転を受け、ユーロフィンがすべてのウイルスクリアランス工程を実施、④レベル4のターンキーサービス(一括サービス)ではフルスケール製造工程の情報を基に、ユーロフィンがスケールダウン工程の開発・バリデーションから、全クリアランス工程の実施までを一括で提供-の4つに分かれて実施する(図)。神戸ラボでは、サービス開始当初はレベル1のみの受託を想定しており、その後、段階的にサービスレベルを拡大していく予定である。
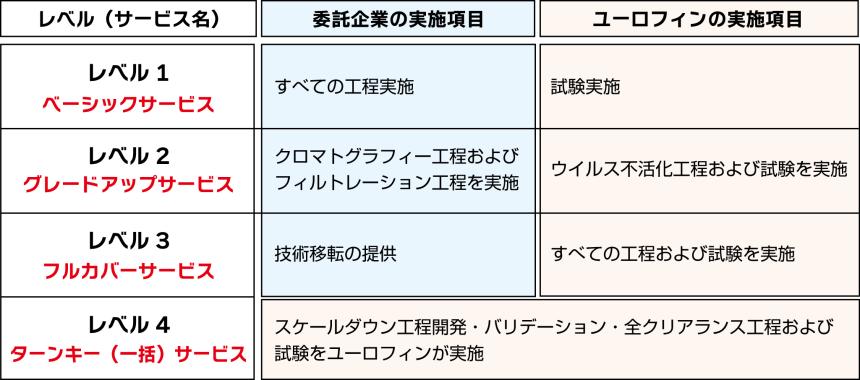
「当社のウイルスクリアランス試験は、バイオ医薬品の安全性確保に不可欠な評価をGMP準拠かつ柔軟な受託体制で提供し、ウイルス選定理由、工程選択の妥当性、LRV(Log Reduction Value)の解釈を含め、CMCドキュメントへの直接的な組み込みを想定したデータ提供が可能であることも強みです。承認申請のスピードアップだけでなく、コスト削減などに寄与するため、サービスを順次拡充させていきます。神戸ラボでは、見学会を実施していますのでぜひ、お立ち寄りください」と金森氏は自信を示す。
ユーロフィン分析科学研究所がウイルスクリアランス試験の国内実施を可能にしたことで、わが国でのバイオ医薬品開発における選択肢がさらに広がったといえるであろう。
●その他の製品・サービスについてはこちらをご覧ください。
■お問い合わせ
ユーロフィン分析科学研究所株式会社
本社(京都ラボ)
〒600-8815 京都府京都市下京区中堂寺粟田町93(京都リサーチパーク内)
神戸事業所
〒650-0045 神戸市中央区港島南町6-7-6(神戸ハイブリッドビジネスセンター内)
E-mail:easl.cserv@bpjp.eurofinsasia.com
URL:https://www.eurofins.co.jp/e-asl/









