─AD─
最短9カ月でバイオ医薬品のFirst-in-Human(FIH)試験へと加速
~細胞株構築からIND申請まで一気通貫のサポート
パセオン(Patheon by Thermo Fisher Scientific)

2025年7月9日、東京ビッグサイトで行われたインターフェックスWeek東京にて、サーモフィッシャーサイエンティフィックによる最新のCDMOソリューション『Path to IND for Biologics』が紹介された。このソリューションは、バイオテクノロジー企業および製薬企業が、DNA配列設計から最終製剤化まで、IND/IMPD申請およびFirst-in-Human(FIH)試験開始に向けた治験薬製造準備を、最短9カ月で実現可能にするというものだ。
本稿では、このソリューションの詳細と具体的な効果について、サーモフィッシャーサイエンティフィックHead of Scientific and Technical AffairsのElena Gontarz氏による講演内容を基に説明する。
■開発迅速化に寄与する“幅広さ”と“細やかさ”
『Path to IND for Biologics』を提供するのは、グローバルにCDMO事業を展開するサーモフィッシャーサイエンティフィックのパセオン(Patheon)ブランドである。同社は原薬・製剤の開発および製造、治験用包装・ラベリング、さらにはコールドチェーン/超低温物流、保管、輸送まで、開発・製造を包括的にサポートする統合ソリューションを提供しており、近年世界有数のCROであるPPDを買収したことで、前臨床から臨床フェーズまでフルスケールで支援できる体制を強化し、まさに医薬品開発を360°全方位的に網羅する『AcceleratorTM Drug Developmen』サービスの提供体制を構築した。グローバルネットワークとグループ内のシナジーを活かしながら、多様なソリューションの展開を可能にしているが、ただサービスの対象が幅広いだけではなく、一つひとつが顧客ニーズに合致したきめ細やかさを持つことも特長だ。
Gontarz氏が講演で紹介した『Path to IND for Biologics』も、まさに“幅広さ”と“細やかさ”という同社のソリューションの特長が表れている。
「IND申請までの工程は多段階かつ長期化しやすく、開発コスト増大の要因となります。そこでわれわれは、バイオ医薬品開発上の障壁となる課題を明確にしてそれぞれを克服することで、開発迅速化とコスト低減につなげています。具体的には、細胞株開発から製剤化、申請支援までを統合したサービスを提供し、FIH試験までのステップを最速化する取り組みを展開しています」と語り、複数の課題解決に資する要素をシームレスにつなぎ合わせることで、開発スピードアップに寄与していることを示唆した。
■AI/ML技術も活用した最先端の細胞株構築ステップ
『Path to IND for Biologics』とは、細胞株構築とトランスポザーゼ技術、多様な分析法プラットフォームなどに加え、テンプレート化された開発計画・報告書、技術移転プロトコルなどを機能的に組み合わせたパッケージであり、これによりIND申請までの期間を短縮できるというものだが、製薬企業はこのサービスをどのように利用することができるか、具体的に見ていきたい。
『Path to IND for Biologics』の起点となるのは、40件以上のIND実績を持つCHO-K1 GSノックダウン細胞株である。Gontarz氏は「この細胞株はIgG1、IgG4、二重特異性抗体、Fc融合体など多様な分子に対応し、最大8g/Lの生産性を実現します」と説明。そして「細胞株構築はAIおよび機械学習(ML)ツールを活用することで、生産性と安定性を最大化するようベクター設計が最適化されています。さらにトランスポザーゼ技術を採用し、発現カセットをゲノムに高忠実度で挿入することで複雑な分子でも安定発現を可能にしており、本技術により複雑な分子構造でも高い力価が得られます」と強調した。
■Beaconシステムによる迅速なクローンのスクリーニング
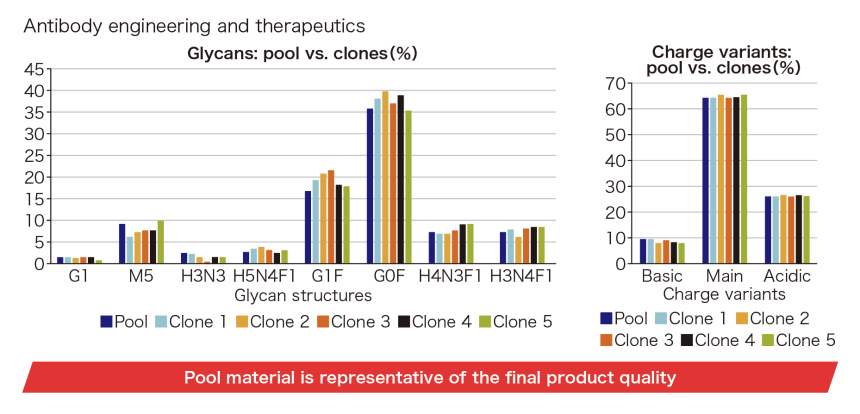
また細胞株開発の成功の鍵を握るもう1つの要素として、Beacon Optofluidic Systemによるクローンスクリーニング工程が挙げられる。このシステムにより、1台の機器による1回の稼働で7,000個のクローンをスクリーニング可能で、さらにNanoPenという技術によって単一クローン性や倍加時間、力価発現を個別評価できる。Gontarz氏は「Beaconで選抜した96クローンを精査・スケールアップし、短期間で最適株を決定できます」と述べるとともに、安定細胞プールと最終クローンの品質がほぼ同一であることを示すデータを提示(図1)。「この特性により、安定細胞プールをプロセス・分析全工程に利用でき、開発期間を大幅に短縮できます」と語った。
■最短9カ月でFIH試験へ、柔軟なスケジュールを選択可能
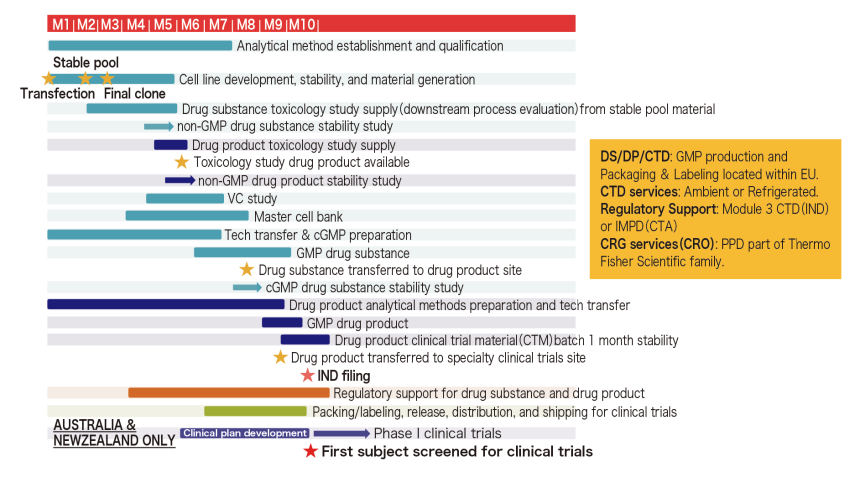
『Path to IND for Biologics』では、下流プラットフォームの評価を簡素化し、毒性試験用原薬に安定細胞プールを使用することで期間を短縮したIgG1/IgG4向けの9カ月スケジュールのサービス(図2)から、毒性試験用原薬の製造に最終クローンを使用し、フルスケールでの下流工程評価を伴うIgG1/IgG4向けの11カ月のスケジュール、二重特異性抗体やFc融合タンパクなどの分子に対応する包括的プラットフォームアプローチによって13カ月でFIH試験入りを可能にするスケジュールなどがある。これらは遺伝子段階からだけでなく、既存の細胞株や安定細胞プールからも開始可能だ。
これほど短期間でFIH試験入りできるのは、プロセス、分析、製剤開発に関するプラットフォーム化を多数行ってきたためだ。「2018年以降で、当社のプロセス開発ラボでは120件を超える多様なプログラムが進行しています」とGontarz氏は語り、世界中で積み上げてきた実績をさらに進化させてプラットフォームに落とし込んでいることを紹介。
「アップストリーム・ダウンストリーム・製剤開発をプラットフォーム化し、Ambr250によるGMPスケールダウン試験、Protein A精製から樹脂スクリーニング、条件最適化まで標準化が進められています。これにより、再現性の高い高品質な成果を確実に実現できる体制が構築されています」と説明した。
■グローバルのネットワークを活かした連携と申請支援
「グローバル拠点間の連携を最大限に活かせる点も、『Path to IND for Biologics』の大きな特長です。プロセス開発、原薬製造、製剤化、包装・ラベル貼付といった一連の工程を、各地域の拠点が密接に連携しながら進めることで、製造から申請準備までを滞りなく進められる体制を整えていることもプロジェクト進行上の大きなメリットです。例えばオーストラリアやニュージーランドではIND不要の場合もあり、製剤出荷後すぐに臨床試験を開始可能ですし、米国・欧州向けにはIND/IMPDパッケージ作成チームが規制申請を支援することで、迅速なFIH試験開始にこぎつけることができます」とGontarz氏。
開発期間を大幅に短縮できるというのが『Path to IND for Biologics』の端的な特長だが、それが科学的裏付けと実績を兼ね備えた開発戦略として、企業の新薬開発プロジェクトに大きな価値をもたらすことが、同氏の講演からわかった。
●その他の製品についてはこちらをご覧ください。
【お問い合わせ】
パセオン株式会社
〒103-0023 東京都中央区日本橋本町 3-3-6 ワカ末ビル 7F
TEL:03-6202-7666
お問合せ・ご質問はこちらより
ウェブサイトはこちらより









