─AD─
Samsung Biologics、ADC開発を加速する分析基盤
プラットフォーム戦略で実現する迅速性と柔軟性
Samsung Biologics
ADC(抗体薬物複合体)の開発では、抗体、リンカー、ペイロードという異なる要素が1つの分子に統合されるため、従来の抗体医薬品以上に高度な分析手法が求められる。しかも近年は、結合様式やペイロードの多様化に加え、IND申請までの時間短縮圧力も強まっており、分析開発部門がプロジェクト全体の成否を左右する局面が増えている。こうした中、Samsung Biologicsは、後期探索から商用生産までをカバーするエンドツーエンド型CDMOとしての事業基盤に、ADC向けのプラットフォーム型分析開発体制を重ね合わせることで、迅速性と再現性、そして分子ごとの最適化を両立する体制を構築している。ADC開発における分析法開発の課題と、Samsung Biologicsにおけるソリューションを紹介する。
■事業基盤の強みは「規模」と「一貫性」
Samsung Biologicsは、後期探索から商用製造までを支援する統合型CDMOとして事業を展開している。Bio Campus I・IIで合計78万5,000リットルの生産能力を持ち、さらに米メリーランド州ロックビルの6万リットルの施設を加えた。対象モダリティも二重特異性抗体、融合タンパク質、ADC、mRNA therapeuticsまで幅広い。加えて、ExellenS™フレームワークのもと、拠点間で標準化された設計、統一プロセス、デジタル化を進め、製造継続性と拠点間同等性を高めている。韓国を中核に、米国、日本へと広がる営業・製造ネットワークも、グローバル案件を意識する顧客にとって大きな魅力だ。
この事業基盤の上に、同社はADC向けの分析開発を「個別対応の寄せ集め」ではなく、プラットフォームとして整備してきた。ADC開発では、分子の複雑さゆえに分析段階がボトルネックになりやすい。そこでSamsung Biologicsは、抗体とADCを一体で捉えるクロスモダリティの分析フレームワークを構築し、初期段階から適用可能性を評価する仕組みを導入している。これにより、プロセス開発や製剤開発と並行して信頼性の高い分析データを生み出し、後工程への橋渡しを円滑にするねらいだ。
■ADC分析の中核は「標準化」と「適応性」の両立
ADCは、抗体に高活性の低分子ペイロードを結合したハイブリッド分子であり、DAR(drug-to-antibody ratio)、遊離薬物やリンカー・ペイロード関連不純物、残留溶媒、ポテンシーといった、ADC特有の重要品質特性を精密に捉える必要がある。Samsung Biologicsは、この複雑さに対し、標準化されたプラットフォーム法を土台にしつつ、各分子の物性や結合様式に応じて調整するアプローチを採用する。分析法開発は「フィージビリティスタディ」「手法最適化」「予備的な分析手法の妥当性確認」「文書化」の4ステップからなる。単一の固定メソッドですべてを測ろうとせず、早期のフィージビリティ評価によってプラットフォームの分析法で、「直接適用可能なもの」と「改良が必要なもの」を峻別するのが特長だ。このようにして本当に必要な場合だけ条件を微調整しながら手法最適化を進めることで無駄な手間や手戻りを減らし、後工程への移管、および規制当局の承認に向けた準備を円滑に進める。同社では具体的なタイムラインとして、分析手法の開発には約3カ月、予備的な分析手法の妥当性確認を1.5カ月ほどで進めると示している(図1)。

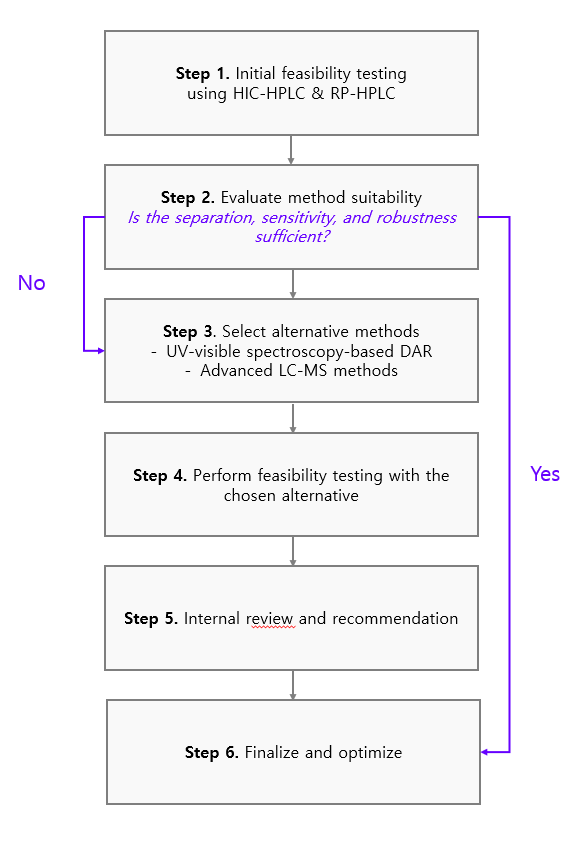
代表例がDAR評価である。DARは各モノクローナル抗体に結合するペイロード分子の平均数で、複数の重要品質特性(CQA)に影響を与えるため、正確かつ移管して測定する必要がある。一方で、ADCは多様化しているため、DARを単一の分析手法で正確に算出することは不可能である。同社はHIC-HPLCとRP-HPLCを基本軸とし、必要に応じてUV-visible DARやLC-MSへ展開する多層的な分析設計を取る。図2では、HIC-HPLCまたはRP-HPLCで初期評価を行い、分離能・感度・頑健性が不十分な場合に代替法へ切り替える判断ツリーが示されている。つまり、最初から過度に複雑な分析に走るのではなく、規制適合性と開発スピードを見極めながら最適法を選定する設計になっている。
遊離薬物やリンカー・ペイロード関連不純物への対応も同社の強みだ。これらは製造過程や保管中に発生し得るうえ、正常組織への毒性に直結するため、微量であっても慎重に管理する必要がある。ペイロードごとに化学構造が異なるため一律の標準化は難しいが、Samsung Biologicsはペイロードクラスごとに調整可能な分析法を開発・整備し、ここでも早期フィージビリティ試験を通じて後戻りを抑える。さらに、ADCのコンジュゲーション工程で用いられる有機溶媒については、GCを用いてDMSO、DMAc、IPAなどを測定し、残留溶媒管理も包括的な分析戦略の中に取り込んでいる。
■細胞ベースアッセイの高速化が差別化要因に
ADCのポテンシー評価では、ELISAのような酵素法に加え、標的結合、細胞内取り込み、細胞傷害活性をより生物学的に反映できる細胞ベースアッセイが重要になる。しかし、この細胞ベースアッセイは、細胞培養準備だけで通常2週間以上を要し、測定にも数日かかるうえ、手技依存性が高く、ばらつきの管理が難しい。このようなことから、細胞ベースのアッセイの開発には膨大な時間とリソースが必要となる。
Samsung Biologicsは、このボトルネックに対してもプラットフォーム発想で標準化と加速化に挑んでいる。複数の細胞株と市販ADCを用いて、96ウェル検出系で共通化できるパラメータを先に標準化し、細胞播種密度やADC濃度範囲など、生物学的特性に依存するパラメータを個別最適化する方式を採用。このように、固定パラメータと可変パラメータをわけた結果、細胞ベースポテンシーアッセイを約3.5カ月で開発・最適化でき、しかもその追加がADC全体の分析開発タイムラインを延ばさないという。
Samsung BiologicsがHIC、LC-MS、RP-HPLC、GCなどのプラットフォーム法を基盤に、ADCの開発で難所となるDAR、遊離薬物、残留溶媒、ポテンシーの4本柱を、IND申請に必要な分析パッケージとして短期間で整え、臨床試験やGMP製造へなめらかにつなぐ体制を作っている。早期フィージビリティ試験で最適法を見極め、反復作業を減らしつつ、細胞ベースアッセイも標準タイムライン内に収めることで、品質とスピードを両立している点が大きな特長だ。ADCの分子設計が多様化し、新規モダリティとしてAOCや抗体ペプチド複合体など次世代バイオコンジュゲートも視野に入る中で、Samsung Biologicsの強みは単なる分析機器の保有ではなく、標準化と適応性を組み合わせた“運用できる分析プラットフォーム”にある。事業規模の大きさと、この分析開発力の組み合わせが、同社のADC CDMO戦略を支える中核になっている。
●関連するホワイトペーパーはこちらをご覧ください

■お問い合わせ
Samsung Biologics
〒21987 大韓民国 インチョン広域市 ヨンス区 ソンド バイオ通り300
TEL:+82-32-455-3114
E-mail:sbio.gsoc@samsung.com
URL:https://samsungbiologics.com









