━AD━
GMPグレードのCPC施設を整備して高品質な細胞の大量培養を実現し、オリジナルのがん免疫細胞の開発から製造までをインハウスで行う医師主導治験へ
ノバ・バイオメディカル

多岐にわたるがん免疫療法の研究開発を牽引し続けている珠玖洋先生(三重大学大学院 医学系研究科 個別化がん免疫治療学 教授)の研究グループ。がんワクチンの開発研究や、リンパ球(とりわけT細胞)を用いた細胞療法の開発に取り組み、動物実験や実験室での研究成果に基づいて、これらの治療法の安全性や有効性を確かめる臨床試験まで、幅広い研究を進めています。
本レポートでは、珠玖先生が取り組まれている研究開発の内容や、インハウスでの製造レベルの細胞培養の実現状況、などについて話を伺いました。
■珠玖先生のチームが長年取り組まれているがん免疫療法について教えてください。
我々は20年以上にわたり、身体の免疫力を高めるがんワクチンや、リンパ球のうちがん細胞を検出して破壊できるキラーT細胞の輸注療法の研究を手がけています。がん免疫療法とは、身体の免疫力ががん細胞の増殖を抑えたり、壊したりできることを利用したものです。
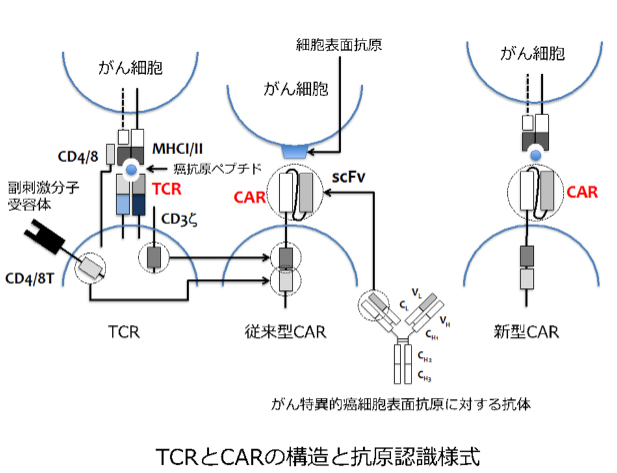
特に後者のT細胞輸注療法として2つの方向の開発を進めています。1つはTCR遺伝子導入T細胞輸注療法。キラーT細胞はT細胞受容体(T cell Receptor:TCR)を発現し、TCRが標的となる細胞を検出します。患者の末梢血から採取したリンパ球に、がん細胞を検出できるTCRの遺伝子をレトロウイルスベクターを用いて導入し、がん特異的なキラーT細胞を人工的に作製します。培養増殖した後に、患者に輸注します。
もう1つはCAR遺伝子導入T細胞輸注療法(CAR-T療法)。がん細胞の表面にある抗原分子に対する抗体遺伝子を改変し、TCRの代わりに用いる手法です。がん細胞表面の抗原を認識する抗体の一部分と、T細胞へ活性化信号を伝える部分を結合したCAR(キメラ抗原受容体)を発現する細胞を作製、培養増殖した後に、患者に輸注します。特に、がん細胞の内部にある抗原分子に由来するペプチドと、MHC分子との複合体が極めてがん特異性に優れていることを利用して、ペプチド/MHC複合体に対する抗体を作製する、新しいCAR治療法の開発を進めています。
■CAR-T療法の課題は、どのようなものですか。
CAR-T療法は、血液がんにおいて優れた治療効果が認められている一方で、固形がんに対する臨床効果が十分に確立していないことが、最大の課題です。3つ理由があります。まず、良い標識抗原の探索が困難なこと。CAR-T療法は、血液がんである急性リンパ性白血病などのCD19という単一の標的分子が、Bリンパ球系腫瘍に有効です。
しかし、がん全体の90%を占める固形がんの場合、適切な抗原を見つけることは簡単ではありません。2つ目に、凝集の状態。血液がんはがん細胞が血流中にばらばらな状態で存在するため、静脈内投与したCAR-T細胞ががん細胞に直接到達しますが、固形がんは組織内に集団状態で存在しており、なおかつ間質と呼ばれる組織が取り囲んでいるため、CAR-T細胞は容易にがん組織内部に到達できません。3つ目に、細胞の栄養であるブドウ糖の取り合い。T細胞が活性化するためにブドウ糖が必要ですが、がん細胞もブドウ糖を消費するため、がん細胞に近いところにいるT細胞が元気を失い、攻撃力が落ちてしまいます。
こうした難点を克服して固形がんに有効なCAR-T療法が実現できれば、適応が増え、多くの患者を救うことにつながります。この方向での開発が、当研究チームを含め世界中で進められています。
■T細胞輸注療法の研究開発には細胞培養の技術が大きなカギを握ると思いますが、
どのような工夫をされていますか。
がん患者の体内のがん特異的なT細胞数は少ないため、患者のT細胞を体外に取り出し、無菌条件下で細胞を10の8乗から10乗レベルの数まで培養増殖し、そうしたT細胞に人工的にがん特異性を付与して体内に戻す治療法がT細胞輸注療法です。患者の体内でよく働き長期間活性を維持できる質の高いT細胞を、大量かつ均一性高く製造する必要があります。その中核として、細胞の培養条件、培養方法は非常に重要です。

まずは、T細胞の最適な培養条件を設定するために、細胞培養において培地中のアミノ酸、グルコースの濃度や細胞代謝産物の測定を行い、細胞が消費する栄養素などをチェックする必要があります。
そして、意図した同じものを作ることができているかという、培養プロセスのモニタリングも行います。代謝状態や活性化状態も見ています。細胞培養は、環境・条件のわずかな差や作業者の技術差により相当な影響が生じます。しかし、細胞療法の実用化のためには、10人の人間が培養したら、10種類の細胞ができるようではだめなのです。
そこで、細胞培養の条件検討や品質管理のために、培養環境の定量的把握を可能とする細胞培養環境分析装置「BioProfile FLEX2」(ノバ・バイオメディカル社製)を採用しています。
■研究室に開設されたGMPグレードのCPC施設の概要について教えてください。
我々は、患者の細胞を採取する医療機関と細胞培養の場所をなるべく近距離にしたほうがよいと考え、培養装置を医療機関のそばに設置する「ディセントラリゼーション(分散型)」を提唱しています。今般の三重大学CPC施設は、このコンセプトを具現化したものです。
医療応用のために、研究室内インハウスに空調管理された清浄エリアであるCPC(Cell Processing Center)を設置し、T細胞などはCPC内で培養します。先述のとおり、培養・製造する細胞は、大量・高品質・均等でなければなりません。標準操作手順書(SOP)をつくって、GMP環境下で違いが生じないように細胞培養するのが大前提ですが、手作業だとどうしても「揺らぎ幅」ができます。
そこで、完全閉鎖式自動培養装置である「クリニマックスプロデジー」(ミルテニーバイオテック社)を導入しています。これにより、T細胞やCAR-T細胞などを完全閉鎖系、GMP環境下で安定的に自動調製できます。約10~14日で細胞を培養して患者に輸注できます。また、完全閉鎖式自動培養装置では、培養条件やプロセスをプログラムとして定義するため、細胞培養の場所が移動したとしても、同等性のある細胞作製ができることになります。製造レベルの細胞培養のために重要な装置なので、日本のメーカーでも完全閉鎖式自動培養装置を開発するところが出てこないかなと思います。
ただし、培養条件の最適化・チューニングにおいては、自動培養装置にプログラムした条件を鵜呑みにすることはありません。目的の細胞の増殖のペース・割合や代謝の状況などはユニフォームなものではなく、プロジェクト成功のためにここをつぶさに見ています。細胞培養プロセスの様々な段階で定期的に上清などをサンプリングして、「BioProfile FLEX2」でチェックしています。代謝項目だけでなく、ガス項目、浸透圧、セルカウンター、電解質といった測定項目を一通りモニタリングします。その結果をよりよい培養条件設定にフィードバックすべく、データを蓄積しています。
■今後の臨床応用へ向けての方針は、どのようなものですか。
現在、オリジナルCAR-T細胞の基礎的な検討、細胞培養の条件検討を終了して、現在は医薬品医療機器総合機構(PMDA)に薬事相談を行っています。2021年9月頃に、三重大学を含む多施設で医師主導臨床試験がスタートする予定です。インハウスで調製した自分たちの細胞が、想定通りに安全で有効性があるかを臨床試験で明らかにします。
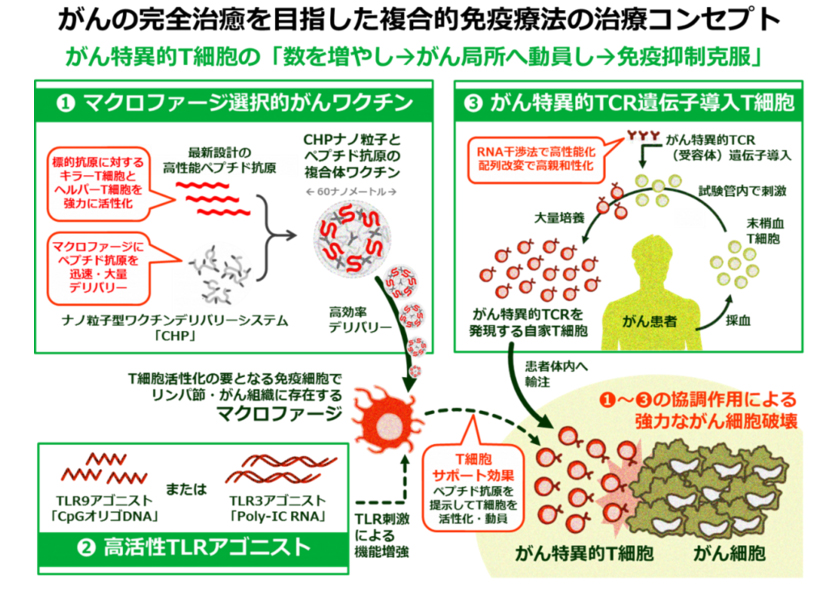
また、がんに対するより有効で安全な治療法としては、いくつか異なった治療法を組み合わせる複合的がん免疫療法を重視しています。これまで開発してきたがんワクチン、T細胞輸注療法を中心に、どのような治療法の組み合わせが有効なのかを検討しています。十数年前からCHP(Cholesterol Hydrophobized Polysaccharides)という多糖類と、がん抗原蛋白との複合体による、我々オリジナルの「CHP-NY-ESO-1 がんワクチン」の開発研究を進めてきました。当該がんワクチンとT細胞輸注療法の組み合わせが極めて強い効果を示すことを発見し、この複合的がん免疫療法の臨床試験を開始しています。
さらに、ここまで述べたがん免疫療法とは厳密には別カテゴリーですが、エクソソームに関する研究もあります。キラーT細胞が産生するエクソソームが、がんの浸潤転移を抑制することを見出しました。複合的がん免疫療法開発の観点では、CAR-T細胞、TCR-T細胞に加えて、エクソソームなども併用オプションと考え、幅広い研究を進めています。
●その他の製品についてはこちらをご覧ください。
■お問い合わせ
ノバ・バイオメディカル株式会社
〒104-6007 東京都中央区晴海1-8-10 晴海アイランドトリトンスクエアオフィスタワーX7F
E-Mail:Jp-info@novabio.com
URL:https://www.novabiomedical.com/jp









