─AD─
大きな市場成長が見込まれる先端医療医薬品(細胞・遺伝子治療、mRNA)の
開発の課題と解決に向けたヒントを探る
パセオン(Patheon by Thermo Fisher Scientific)
■積極的な投資でビジネス基盤を強化
サーモフィッシャーサイエンティフィクのパセオンファーマサービシズ(以下パセオン)は、低分子からバイオ医薬、さらには、細胞・遺伝子治療やmRNAまでを対象に、世界で顧客のサポートを続けるグローバルCDMOだ(図1)。
分析、ラボ製品、バイオリアクターや培地開発など多様なセクションがあるサーモフィッシャーグループ内でのシナジーを活かしつつ、積極的な投資で技術力強化と体制整備を進めており、2019年より約30億ドル規模の投資を行って企業買収を進めてきた。
CDMOサービスを手掛けるパセオンの特長は、長い医薬品開発過程の中で、前臨床の段階から上市後の商用生産まですべてをカバーしていることが挙げられる。さらに治験薬包装やラベリング、保管・配送まで対応するなど、その網羅性で他のCDMOの追随を許さない唯一の存在となっているが、そんなパセオンは近年、注目を集める先端医療医薬品領域にも注力している。

■大きな成長が期待される市場、充実した施設で対応
現在、開発中の細胞・遺伝子治療やmRNAが増えているが、CMC、同等性/同質性、分析法、生産能力や人材確保などクリアすべき課題が多々あり、開発難度が高いのが現状だ。ただ一方で、多額の投資が行われており、伸びしろが大きいマーケットとして捉えることもでき、いかに開発過程での課題をクリアするかが成功の鍵になっている。このように規模が一気に拡大することが期待される市場において、パセオンもCDMOビジネスを積極的に拡大しているのだ。
では、それら課題に対してパセオンはどのような解決のアプローチをとっているのだろうか?前述のようにCMCや同等性、分析法確立や生産能力確保など、開発上の課題は多岐に渡り、どれか1つの要素をクリアするだけで克服するのは難しい。そこでパセオンはここ数年、これらの技術力全体を向上させるべく多額の投資を行ってきたのだ。大きなものでは、2019年に米国のウイルスベクターCDMOであるブラマーバイオ(Brammer Bio)を買収し、これをきっかけに本領域に参入し、さらにプラスミドDNAの工場設立や細胞・遺伝子治療の設備にも積極的に投資した。そして、2021年には ヘノジェン(Henogen)を買収し、欧州(ベルギー)にも製造拠点を持つことになった。ブラマ―バイオやヘノジェンはウイルスベクターのCDMOとして20年以上の実績をもつため、設備、人材、知識などのノウハウをそのまま活かせるのは強みだろう。
パセオンは現在、細胞・遺伝子治療領域で世界に15施設を有する。また米国のマサチューセッツ州プレインビルでは世界トップクラスのキャパシティをもつウイルスベクター製造施設が稼働しており、イタリアのモンツァの注射剤の開発・製造工場の中に、さらにmRNAの原薬からLNP にも対応するエンドツーエンドサービスを追加し、対応サービス範囲を拡張した。
これら先端医療医薬品に関するトランスレーショナルサービスでは、基礎研究段階からGMP製造を念頭に置いて標準化されたプロセスや的確な分析法を構築することで、将来の治験薬製造および商用生産への移行におけるリスクを回避し円滑に進めることが可能となった。サーモフィッシャーの革新的な技術と充実したインフラを駆使しプロセスおよび分析法開発の支援から前臨床に向けたPOCデータ作成に至るサービスを提供している。
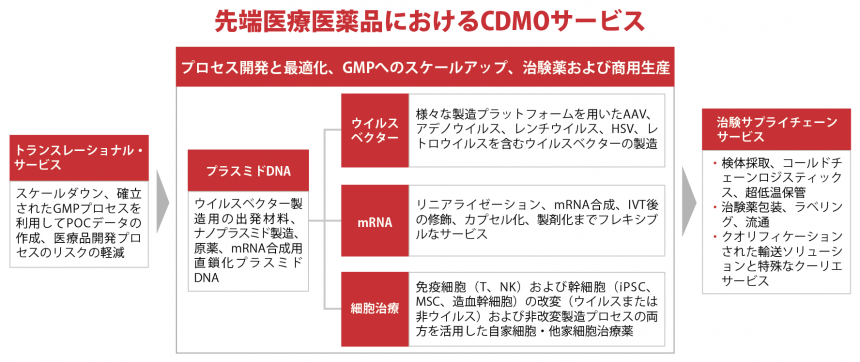
さらにこうした製造設備の充実とともに、本領域でもエンドツーエンドサービスを実現していることもパセオンの大きな特長だ。図2にパセオンの先端医療医薬品に関する対応範囲を示したが、温度管理が厳しい製品の増加にあわせて、治験薬、上市品ともに超低温での保管・輸送にも対応しているなど、顧客ニーズと製品特性に合わせてサービスを進化させていることもうかがえる。
■IND申請の迅速化に向けたパセオン独自の初期開発プログラム
開発競争が激化している中で、迅速に市場に製品を投入することが必須となり、複雑な分子構造をもつウイルスベクター製品の開発を進めるには、開発初期段階からGMPへのシームレスな移行に必要な品質と製造方法を念頭に置くという全体を見通す視野が必要となるが、パセオンはリード候補物質特定段階からサポートし、その後の前臨床、GMP、商業生産への移行を円滑に行う豊富な実績を有している。その1つの課題解決として、 開発にプラットフォームプロセスを用いて、プロセスバリデーションや技術移管の必要範囲を最小限に抑え、バッチ記録の標準化、逸脱の低減、規制対応でのリスク排除によって早期臨床入りとコスト削減の両立を提供しているのだ。
その中で前臨床から治験薬製造までの段階におけるパセオン独自の「ウイルスベクター Quick to ClinicTM」プログラムを紹介する。このプログラムでは、ウイルスベクター、アデノ随伴ウイルス(AAV)やレンチウイルス(LV)の浮遊系製造などの条件に制限があるが、長年培ったウイルスベクターの開発・GMP製造の経験を元に開発されたプラットフォームを使い、標準化された文書を利用する。それによって、少ないコストや短いタイムラインでグローバル治験に向けてサポートし、初期開発の加速化に貢献する。このプログラムを活用することで、全体を統合に管理し、必要なステップ数を削減することで、標準的なプロセスに比べて6カ月以上の開発期間短縮を実現するという。
■規制対応・申請業務でも顧客の負担を軽減
さらにウイルスベクターQuick to ClinicTMプログラムでは規制対応サポートも充実している。米国、欧州、カナダ、日本の規制当局へのIND申請および承認申請をサポートする、豊富な経験を持つ専門家チームがあり、余剰な業務を省いたリソースの削減、効率的な申請準備を可能にする電子文書管理システムの活用などを通じ、規制対応業務を強力にサポートすることが可能。製品を市場に送り出すには、技術的要素だけでなく規制当局への申請も大きな壁になるが、それらを手厚いサポートで乗り越える体制を同社は整えているのだ。
ウイルスベクター製造に関する20年以上の経験の中で、治験用・商用ウイルスベクターのGMP製造実績は700ロット以上にものぼり、現在米国と欧州において2品目の商業ライセンスの取得をしている。また細胞・遺伝子治療の開発・製造・サプライチェーンのグローバルネットワークも整備されるなど、グローバルでビジネスを展開する上での課題解決に資する要素を網羅しているといっても過言ではない。
設備の充実、提供サービスの幅広さ、規制対応を含めたサポートの深さを持つパセオン。これから大きく花開く先端医療医薬品領域の市場で、同社が提供する価値が業界屈指のものであるといえるだろう。
●その他の製品についてはこちらをご覧ください。
【お問い合わせ】
パセオン株式会社
〒103-0023 東京都中央区日本橋本町 3-3-6 ワカ末ビル 7F
TEL:03-6202-7666
ウェブサイトはこちらより
ご相談・お問合せはこちらより









