GMP準拠のサイトカイン製品
IL-15、IL-7、IL-21など、様々な高品質のGMP準拠サイトカインの開発に成功しております。免疫細胞治療薬の臨床研究をサポートし、医薬品規制当局の承認を加速できます.
2023/06/20
CAR-T/NKを初めとする免疫細胞治療は、白血病、リンパ腫、多発性骨髄腫など、様々な悪性腫瘍の治療に著しい治療効果を示しており、世界中から注目を集めています。現在では、数多い細胞治療薬がFDAによって承認されています。免疫細胞療法が臨床試験や販売申請に進むと、製品の品質や製造管理に関する規制が必要となります。免疫細胞治療製品の製造工程において、IL-15、IL-7、IL-21などの培地サプリメントがT/NK免疫細胞の増殖と分化の主な試薬であり、免疫細胞治療薬の製造の主要な原料です。このように、免疫細胞治療薬の開発・販売を成功させるためには、安全で効果的かつ規制を満たすサイトカインが不可欠です。
ACROBiosystemsは、免疫細胞治療薬の臨床応用で使用できる高品質の試薬の開発に取り組んでおります。さらに、生産体制としては、GMP準拠の品質管理システムプラットフォームを利用し、細胞治療薬の製造規制と厳格な品質管理基準に従い、合格した製品だけを市場に送り出しております。当社はIL-15、IL-7、IL-21など、様々な高品質のGMP準拠サイトカインの開発に成功しております。免疫細胞治療薬の臨床研究をサポートし、医薬品規制当局の承認を加速できます。
*弊社のGMP準拠の製品は、研究開発、製造、またはin vitroでの使用を目的としておりますが、人間に直接使用することはできません。
当社のGMP準拠品質管理システム
ISO 9001:2015とISO 13485:2016認証取得
いずれの工場でも医薬品製造承認を取得
医薬品B+Aレベルのクリーンルームと自動充填装置
無菌操作と二次滅菌ろ過
動物由来成分フリー
スタッフに厳しいトレーニングを実施
サプライヤーと原材料の管理
QA基準を満たす品質/製造過程
全ての工程を記録し、監視されています
機器のメンテナンスと校正を定期的に実施
分析法は検証済み
Regulatory Support Files (RSF) を提供可能
品質管理を厳格に実施
(IL-15を例とする)
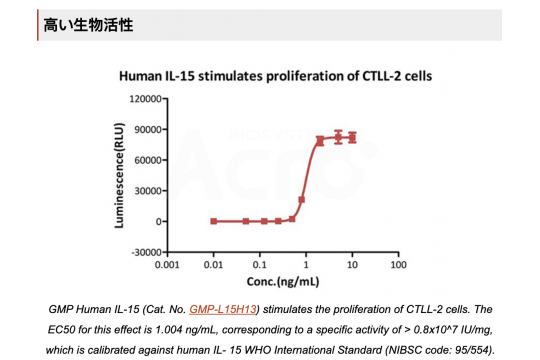
生物活性>0.8 x 107 1U/mg
純度>95%
エンドトキシン<10EU/mg
残留宿主細胞のDNA含有量は0.02ng/μg未満
残留宿主細胞タンパク質含有量は0.5ng/ug未満
無菌試験
マイコプラズマの検出
外因性ウイルスの検出
ロット間の一貫性は良好
高い安定性が確認されています (加速試験、凍結融解試験、長期保存試験、輸送期間の安定性)